本导基因全球首个基因编辑抗病毒疗法开启高剂量组患者招募
发布日期:2024-08-20
全球首个体内基因编辑抗病毒疗法BD111治疗病毒性角膜炎一期试验患者招募持续进行中,该临床试验正在温州医科大学附属眼视光医院、浙江大学医学院附属第二医院和复旦大学附属华山医院开展,最后一个剂量组的患者招募按计划启动。
单纯疱疹病毒(HSV)是人类最常见的病原体。其唯一的自然宿主,就是人类。因此,HSV在人群中的感染极为普遍,至今仍是尚未被攻克的医学难题,既无疫苗可用,也无药物可以根治。
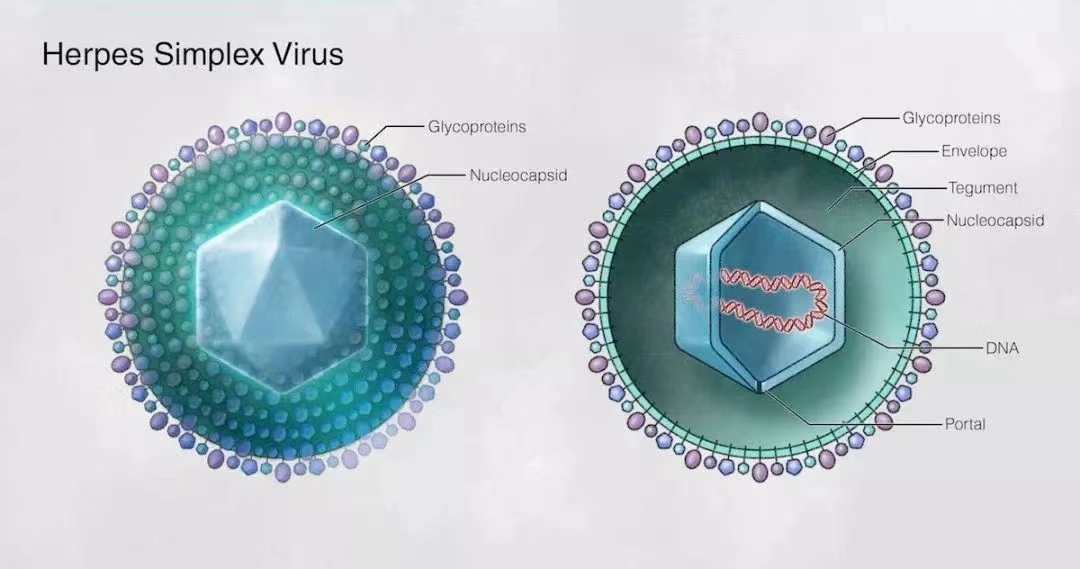
单纯疱疹病毒性角膜炎(herpes simplex keratitis)是由单纯疱疹病毒(herpes simplex virus,HSV)感染引起的病毒性角膜炎,为临床较常见的致盲性角膜疾病之一。针对中国人群的流行病调查研究结果显示,其发病率约为65/10 万至110/10万。其中,I型单纯疱疹病毒性基质型角膜炎是最难治疗的临床亚型。
单纯疱疹病毒性角膜炎临床治疗的痛点
1.持续多年的反复复发,给患者带来较大身心痛苦;
2.虽有临床治疗药物,但只能抑制病毒繁殖暂时缓解病情,不能彻底清除残存病毒,当患者免疫低下时,病毒重新繁殖、病情复发;
3.常年复发的药物治疗,一方面长期用药带给患者生活不便,另一方面也带来耐药和药物不良反应风险;
4.反复的病情发作,容易造成角膜的瘢痕形成、新生血管化、角膜穿孔等,是临床上较为常见的致盲眼病之一;
5.目前,全球缺乏治愈性疗法或药物;
6.研究发现HSV病毒也与阿尔兹海默症存在关联。
研发治愈性先进疗法减少甚至避免复发,是当前复发性I型单纯疱疹病毒性基质型角膜炎临床治疗的急需。
BD111注射液由上海本导基因技术有限公司(以下简称本导基因)研发,是国家药监局批准的中国首个体内基因编辑临床研究,也是全球首个基因编辑抗病毒疗法。此外BD111还获美国FDA临床研究批件以及孤儿药资格。
- 2024年7月:由上海交通大学蔡宇伽教授(本导基因创始人)团队联合丹麦科学家团队首次发现神经元特有的HSV-1病毒限制性因子TMEFF1,揭示大脑对抗病毒感染的独特机理,论文发表于《Nature》(2024; on line.);
- 2021年1月:由上海交通大学蔡宇伽教授(本导基因创始人)团队完成HSK动物疾病模型的初步药效学验证(POC),论文发表于《Nature Biotechnology》(2021; 39(5):567-577.);
- 2023年11月:复旦大学附属眼耳鼻喉科医院洪佳旭教授牵头完成BD111治疗难治性HSK患者的研究者发起的临床研究(IIT)。论文发表于美国基因与细胞治疗协会(ASGCT)会刊《Molecular Therapy》(2023; Nov 1;31(11):3163-3175.);
- 2022年3月18日:在第七届医学家年会(2022)暨第二届医师职业发展论坛上,中国医师协会眼科医师分会会长、北京同仁医院王宁利教授发布了2021年度“中国眼科学十大进展”,BD111位居榜首。
本导基因于2023年4月28日正式获得国家药品监督管理局(NMPA)BD111治疗复发性I型单纯疱疹病毒性基质型角膜炎1/2a期临床试验批件(2023LP00775),试验项目名称为:
目前,BD111一期临床试验即将开始高剂量组的受试者招募。BD111在前3个剂量的受试者中表现出了较好的安全性和耐受性,未发生任何严重不良事件和剂量限制性毒性事件;短期内疗效也有了令人希望的结果。
通过PUBMED、EMBASE、Clinical trial网站、FDA网站、EMA网站及ChatGPT等工具的信息搜索,目前全球有三款在研抗HSV基因编辑疗法,除了本导基因研发的BD111注射液,其他两款均由美国研发(一款是美国Fred Hutchinson癌症中心开发的基因治疗候选产品;一款为Excision Bio的EBT-104)。本导基因BD111无论在技术水平和研发进度上均有显著的优势。三者比较如下表:

BD111注射液:全球首个进入临床阶段的体内基因编辑抗病毒药物(first-in-class),也是全球首个进入临床阶段的类病毒体VLP技术。
同类竞品情况:同类竞品还处于临床前的动物研究阶段,尚未完成IND申报的GLP级别的研究。从研发进度上讲,与BD111注射液相比最少相差3年甚至更长的时间。
目前,该临床试验正在温州医科大学附属眼视光医院、浙江大学医学院附属第二医院和复旦大学附属华山医院开展,最后一个剂量组的患者招募持续进行中。
如您初步符合以下条件,且愿意了解此临床研究,即可与我们联系:
本导基因是一家以体内基因编辑治疗为特色的基因治疗创新药物研发企业,致力于为眼科、神经系统、造血系统、病毒感染以及肿瘤等多领域的难治性疾病开发具有全球意义的创新药物。本导基因拥有国际领先VLP mRNA递送平台(BD-VLP)和下一代慢病毒载体平台(BDlenti)。围绕着核心递送技术平台,本导基因布局了多条First-in-Class的产品管线,开展了多项First-in-Human临床研究;基于两大核心递送技术的管线BD111和BD211均进入了正式临床阶段。本导基因与国际著名药企开展了重大神经系统疾病新型基因疗法的合作研发,是国内基因治疗领域的头部企业。本导基因在国际上率先开展了体内基因编辑抗病毒治疗的临床研究,在β-地中海贫血、青光眼和老年黄斑变性的基因治疗上也取得了重要的临床突破。公司核心技术发表于Nature Biotechnology、Nature Biomedical Engineering等国际权威期刊。公司拥有4000 平的GMP中试基地和研发基地。与上海交通大学系统生物医学研究院共建了“基因治疗联合研发中心”。本导基因秉持“稳扎稳打、锐意创新”的企业精神,立足中国,服务世界,为重大难治性疾病提供首创性解决方案!
